A alopecia fibrosante frontal (AFF) é uma alopecia cicatricial linfocítica primária com etiopatogenia obscura. Já foram propostas hipóteses hormonais, imunomediadas, genéticas e ambientais; uma delas está relacionada ao aumento do uso de filtro solar.1 O objetivo do presente estudo foi identificar uma possível associação entre AFF e o uso de filtro solar nessa população de pacientes.
Este foi um estudo de caso‐controle com 36 mulheres hispânicas; 18 casos e 18 controles foram pareados por sexo e idade. O protocolo foi aprovado pelo Comitê de Ética local do Hospital Universitario Dr. José Eleuterio González, em Monterrey, México. Foi elaborado um questionário com perguntas sobre produtos de higiene e protetores solares, incluindo o tempo de uso. Pacientes e controles foram testadas com adesivos utilizando alérgenos das séries AllergyEAZE Standard, Cosmetic e Photopatch. As leituras foram realizadas 48 e 96 horas após a aplicação. As reações foram medidas pelos critérios do North American Contact Dermatitis Group.2 Pacientes com AFF atendidas em nossa clínica de dermatologia no período de 2012 a 2018 foram incluídas no estudo. O teste exato de Fisher foi utilizado para comparar os grupos. A significância estatística foi considerada com p <0,05.
A média de idade foi de 59,1 para as pacientes com AFF e de 56,5 anos para as controles. Dezesseis casos estavam na pós‐menopausa. Dez pacientes relataram sintomas mínimos (principalmente prurido). Sete casos apresentavam pelo menos uma doença autoimune; líquen plano pigmentoso foi a mais comum. Nove pacientes tinham história familiar de autoimunidade.
Alopecia fora do couro cabeludo foi observada em 15 casos. Todos tinham envolvimento de sobrancelha; 12 casos, de membros; e 10, de cílios. Oito indivíduos apresentavam pápulas faciais.
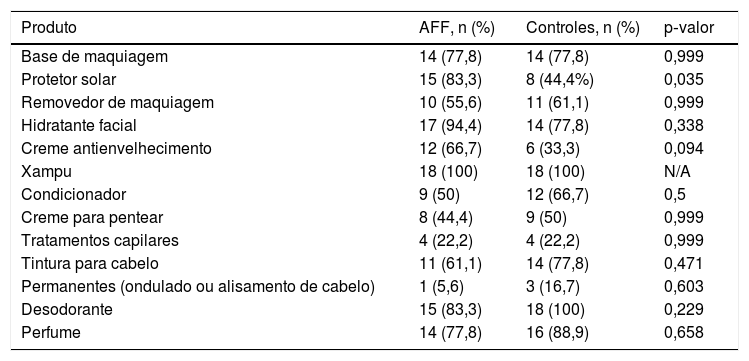
A tabela 1 descreve o uso de produtos de higiene. O uso de filtro solar em pacientes com AFF foi quase o dobro do que nos controles saudáveis (p=0,035). Base de maquiagem era utilizada por 14 mulheres em cada grupo. Os casos de AFF usavam mais hidratantes faciais em comparação com os controles, sem significância estatística.
Produtos de higiene pessoal utilizados por casos e controles
| Produto | AFF, n (%) | Controles, n (%) | p‐valor |
|---|---|---|---|
| Base de maquiagem | 14 (77,8) | 14 (77,8) | 0,999 |
| Protetor solar | 15 (83,3) | 8 (44,4%) | 0,035 |
| Removedor de maquiagem | 10 (55,6) | 11 (61,1) | 0,999 |
| Hidratante facial | 17 (94,4) | 14 (77,8) | 0,338 |
| Creme antienvelhecimento | 12 (66,7) | 6 (33,3) | 0,094 |
| Xampu | 18 (100) | 18 (100) | N/A |
| Condicionador | 9 (50) | 12 (66,7) | 0,5 |
| Creme para pentear | 8 (44,4) | 9 (50) | 0,999 |
| Tratamentos capilares | 4 (22,2) | 4 (22,2) | 0,999 |
| Tintura para cabelo | 11 (61,1) | 14 (77,8) | 0,471 |
| Permanentes (ondulado ou alisamento de cabelo) | 1 (5,6) | 3 (16,7) | 0,603 |
| Desodorante | 15 (83,3) | 18 (100) | 0,229 |
| Perfume | 14 (77,8) | 16 (88,9) | 0,658 |
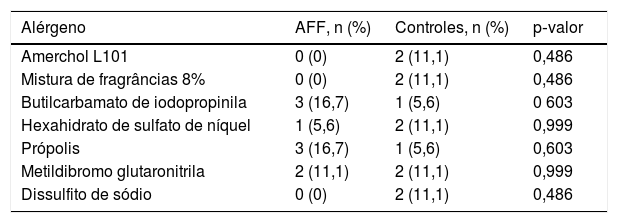
Reações positivas a pelo menos um alérgeno ocorreram em 15 pacientes, contra 10 controles; nenhuma diferença significativa foi encontrada. Os alérgenos mais comuns em AFF foram butilcarbamato de iodopropinila e própolis (tabela 2). Os produtos de higiene das pacientes foram revisados, e recomendações foram feitas para evitá‐los.
Alérgenos de contato positivos mais comuns
| Alérgeno | AFF, n (%) | Controles, n (%) | p‐valor |
|---|---|---|---|
| Amerchol L101 | 0 (0) | 2 (11,1) | 0,486 |
| Mistura de fragrâncias 8% | 0 (0) | 2 (11,1) | 0,486 |
| Butilcarbamato de iodopropinila | 3 (16,7) | 1 (5,6) | 0 603 |
| Hexahidrato de sulfato de níquel | 1 (5,6) | 2 (11,1) | 0,999 |
| Própolis | 3 (16,7) | 1 (5,6) | 0,603 |
| Metildibromo glutaronitrila | 2 (11,1) | 2 (11,1) | 0,999 |
| Dissulfito de sódio | 0 (0) | 2 (11,1) | 0,486 |
Aldoori et al.3 sugeriram fatores ambientais associados à AFF, com uma diferença significativa no uso de filtro solar em comparação com os controles. Eles realizaram testes de contato em 40 pacientes; foram encontradas mais reações positivas ao hidroperóxido de linalol e ao bálsamo do Peru em indivíduos com AFF quando comparados a indivíduos testados com adesivos em geral. Rocha et al.4 não observaram diferenças em 63 pacientes com AFF em comparação com indivíduos testados com adesivos locais; fotoalergia não foi detectada. Os alérgenos identificados na AFF são incapazes de explicar a associação entre a doença e o uso de protetor solar.5 Thompson et al.6 encontraram nanopartículas de dióxido de titânio (TiO2) em fios de cabelo de pacientes com AFF e controles assintomáticos; não foram encontradas reações positivas em testes de contato realizados em oito pacientes com AFF utilizando cinco tipos de titânio. Não está claro se o TiO2 desempenha um papel na patogênese da AFF. Recentemente, Rudnicka et al.7 analisaram testes de contato em 20 pacientes com AFF e 24 controles saudáveis e encontraram reações positivas nos testes de contato a um ou mais alérgenos em 65% dos casos, enquanto apenas 37,5% dos controles tiveram uma reação positiva. Os alérgenos mais comuns encontrados no grupo AFF foram cloreto de cobalto hexa‐hidratado 35%, sulfato de níquel hexa‐hidratado 25%, e dicromato de potássio 15%. Em nosso estudo, 83,3% dos casos e 55,5% dos controles apresentaram pelo menos um alérgeno com reação positiva.
O presente estudo incluiu controles saudáveis pareados por sexo e idade, enquanto a maioria das publicações anteriores utilizou uma população geral nos testes de contato. As limitações incluem o pequeno tamanho da amostra, viés de memória para uso de filtro solar, falta de estudos genéticos e generalização em decorrência da homogeneidade racial/étnica.
Em conclusão, a etiopatogenia da AFF permanece desconhecida. Aumento do uso de filtro solar e maior prevalência de alergia de contato foram demonstrados neste estudo nos pacientes com AFF, levantando a questão de que as respostas alérgicas/imunológicas em pacientes geneticamente predispostos poderiam ser desencadeadas por substâncias exógenas. A maior prevalência estatisticamente não significativa de alergia de contato no presente estudo e a heterogeneidade de resultados em estudos anteriores endossam a necessidade de novas pesquisas para confirmar essa associação.
Suporte financeiroNenhum.
Contribuição dos autoresSonia Sofia Ocampo‐Garza: Concepção e planejamento do estudo; obtenção, análise e interpretação de dados; redação do manuscrito; aprovação da versão final submetida.
Maira Elizabeth Herz‐Ruelas: Concepção e planejamento do estudo; Análise e interpretação de dados; revisão do manuscrito; aprovação da versão final submetida.
Sonia Chavez‐Alvarez: Concepção e planejamento do estudo; revisão do manuscrito; aprovação da versão final submetida.
David Marcelo de la Fuente‐Rodriguez: Obtenção de dados; aprovação da versão final submetida.
Jorge Ocampo‐Candiani: Concepção e planejamento do estudo; Análise e interpretação dos dados; revisão do manuscrito; aprovação da versão final submetida.
Conflito de interessesNenhum.
Como citar este artigo: Ocampo‐Garza SS, Herz‐Ruelas ME, Chavez‐Alvarez S, Fuente‐Rodriguez DM, Ocampo‐Candiani J. Association of frontal fibrosing alopecia and contact allergens in everyday skincare products in Hispanic females: a case‐control study. An Bras Dermatol. 2021;96:776–8.
Trabalho realizado no Hospital Universitario Dr. José Eleuterio González, Monterrey, NL, México.