O vitiligo é doença comum com uma carga elevada, e o tipo recalcitrante não responde aos tratamentos médicos atuais. O enxerto autólogo de melanócitos não cultivados e tripsinizados, procedimento simples e baseado em experiências, tem sido sugerido para o tratamento do vitiligo.
ObjetivoAvaliar o o emprego do enxerto autólogo de melanócitos não cultivados e tripsinizados no vitiligo recalcitrante.
MétodosEste ensaio clínico foi realizado em 28 pacientes (20 mulheres e 8 homens). Após a demarcação e a preparação das áreas doadoras e receptoras, ambas as áreas foram abrasadas utilizando‐se uma cureta. Os materiais colhidos do sítio doador foram tripsinizados e centrifugados. A suspensão resultante foi misturada com gel de ácido hialurônico e distribuidas sobre a área receptora abrasada.
ResultadosForam incluídos em nosso estudo 28 pacientes, com um total de 108 lesões e média de idade de 25,93 ± 7,11 anos. Vitiligo generalizado (57,1%) foi o tipo clínico mais comum, e a face e a região cervical (38%) os locais mais frequentemente tratados. Repigmentação boa a excelente foi observada na face e região cervical, no tronco, na extremidade superior e na área genital em 31 (57,4%), 11 (20,4%), 9 (16,7%) e 3 (5,5%) pacientes, respectivamente. A face e a região cervical apresentaram resultados significativamente melhores (p < 0,05).
Limitações do estudoPequeno tamanho amostral e estudo de centro único.
ConclusãoO enxerto autólogo de melanócitos não cultivados e tripsinizados é um método seguro e com resultado satisfatório no vitiligo recalcitrante. O adequado treinamento dos médicos e a experiência dos especialistas no emprego do método podem ser determinantes para aumentar a taxa de sucesso.
O vitiligo é dermatose pigmentar comum que está associado a vários contextos, como educação, família, casamento, emprego, sexo e relações sociais.1–4Não há cura definitiva para o vitiligo; portanto, muitas opções cirúrgicas, como enxerto autólogo de melanócitos cultivados ou não cultivados, foram desenvolvidas para seu tratamento nos últimos anos.3,5–13No vitiligo recalcitrante (VR), incluindo vitiligo em áreas com pelos com leucotríquia ou em áreas glabras, a doença é resistente ao tratamento e requer intervenções cirúrgicas, como enxerto autólogo de melanócitos não cultivados e tripsinizados (ANTMG; do inglês, autologous non‐cultured and trypsinized melanocyte grafting).5,7,9,14–18Em virtude da alta prevalência do vitiligo e dos muitos problemas psicossociais com alto custo de tratamento, o ANTMG foi utilizado para o tratamento do VR.
Materiais e métodosDesenho e população do estudoEste estudo intervencionista e de seguimento foi realizado em 31 pacientes por um período de 18 meses, de 2019 a 2020, na Clínica de Referência em Dermatologia Hajdaie da Kermanshah University of Medical Sciences, Irã. O procedimento ANTMG e o seguimento foram realizados em 28 dos 31 pacientes; três pacientes foram excluídos do estudo. Os pacientes foram selecionados entre os encaminhados à clínica.
Foram recrutados pacientes com vitiligo documentado clinicamente por dois dermatologistas que não faziam parte do presente estudo. Além disso, os pacientes não podiam apresentar lesão de vitiligo nova ou aumentada pelo menos nos últimos seis meses, apresentar pelo menos três manchas, lesões de vitiligo menores que 100cm2, lesões em áreas glabras ou em áreas não glabras com leucotríquia, e não responsividade ao tratamento atual nos últimos dois anos. Lactantes e gestantes, pacientes com menos de 15 ou mais de 60 anos de idade e pacientes com história positiva de fenômenos de Koebner, queloide ou cicatriz hipertrófica, imunodeficiência, distúrbios psicológicos, infecção ativa no sítio receptor ou doador e vitiligo instável e universal foram excluídos do estudo.
Informações abrangentes sobre ANTMG foram fornecidas a todos os pacientes. Em seguida, foi obtido o consentimento por escrito e os pacientes foram finalmente incluídos no estudo, aprovado pelo Comitê de Ética da Kermanshah University of Medical Science e registrado no banco de dados Iranian Registration Clinical Trial (IRCT; IRCT20130812014333N146). As informações dos participantes foram mantidas em sigilo.
ProcedimentoEscolhemos as áreas laterais das coxas ou dos glúteos com cor de pele normal como sítios doadores. Considerou‐se a área do sítio doador um quarto do sítio receptor (fig. 1).
O sítio doador selecionado foi demarcado e anestesiado com injeção de lidocaína a 2% sem epinefrina. Então, foi utilizada uma cureta descartável e cortante n° 2 para a coleta dos materiais autólogos. A amostra coletada foi transferida para um recipiente e triturada com lâmina de bisturi n°10. Em seguida, o material colhido foi incubado com tripsina em concentração muito baixa (0,25%) por 10 minutos a 37°C. Em seguida, para sua inibição, utilizou‐se 100μL de soro do paciente, sendo então lavado com soro fisiológico (fig. 2).
Para obter uma suspensão apropriada, a solução processada foi centrifugada. A amostra do material resultante foi preparada como esfregaço direto e avaliada em microscópio óptico para demonstrar a presença de melanócitos.
A raspagem das manchas despigmentadas receptoras foi feita de maneira semelhante ao realizado nos locais doadores com injeção local de lidocaína e uma cureta semelhante à utilizada nos locais doadores. Os materiais colhidos e processados foram misturados ao ácido hialurônico Revofil (23mg/mL) na proporção de 5:1 e foram distribuídos uniformemente nos áreas receptoras. O sítio receptor foi coberto com um curativo semipermeável (Tegaderm) e o sítio doador foi coberto com gaze e pomada de tetraciclina. Foi prescrito aos pacientes antibiótico oral (cefalexina 500mg a cada 6 horas) por uma semana após o procedimento. Os pacientes também foram orientados a imobilizar o sítio receptor por uma semana. O curativo da área doadora foi trocado diariamente pelo paciente, mas o curativo da área receptora foi trocado e substituído pelo pesquisador após uma semana.
O paciente foi avaliado na primeira e terceira semanas, no segundo mês e depois a cada dois meses durante 18 meses. A taxa de repigmentação das áreas tratadas foi calculada ao longo de 18 meses, onde a repigmentação estava estacionária em todos os pacientes, com base nas fotografias pré e pós‐operatórias, por dois dermatologistas não envolvidos neste estudo. A porcentagem de repigmentação e possíveis complicações foram registradas nos prontuários dos pacientes.
A repigmentação foi classificada como pigmentação excelente (mais de 75%), boa (50%–74%), moderada (25%–49%) e fraca (menos de 25%) nas regiões tratadas.
Análise estatísticaOs dados coletados foram analisados com o software SPSS V22. Para comparar as variáveis qualitativas em dois grupos, utilizou‐se o teste do qui‐quadrado ou exato de Fisher, e p < 0,05 foi considerado significativo.
ResultadosDos 28 pacientes, 20 (71,4%) eram do sexo feminino e oito (28,6) do sexo masculino, com média de idade de 25,93 ± 7,11 anos e 108 manchas de vitiligo.
O intervalo de duração da doença foi de dois a 12 anos, com duração média de 5,14 ± 3,2 anos. Dos pacientes, 12 (42,9%) tinham história familiar de vitiligo (tabela 1).
Características demográficas e clínicas dos pacientes do presente estudo
| Variáveis | |
|---|---|
| Número de pacientes (n) | 28 |
| Número de manchas de vitiligo, n (%) | 108 |
| Média de idade dos pacientes (anos) | 25,93 ± 7,11 |
| Sexo | |
| Feminino, n (%) | 20 (71,4%) |
| Masculino | 8 (28,6%) |
| História familiar, n (%) | |
| Positiva | 12 (42,9%) |
| Negativa | 16 (57,1%) |
| Duração média da doença (anos) | 5,14 ± 3,2 |
| Tipo de vitiligo, n(%) | |
| Focal | 4 (14,3%) |
| Segmentar | 8 (28,6%) |
| Acrofacial | 4 (14,3%) |
| Vulgar | 12 (42,8%) |
| Locais afetados, n (%) | |
| Extremidade superior | 17(60,7%) |
| Face e região cervical | 17(60,7%) |
| Tronco | 12 (42,8%) |
| Extremidade inferior | 8 (28,6%) |
| Área genital | 2 (7,1%) |
| Locais tratados, n (%) | |
| Face e região cervical | 41(38,0%) |
| Extremidade superior | 19 (17,6%) |
| Tronco | 37 (34,2%) |
| Área genital | 11 (10,2%) |
Quanto ao tipo de vitiligo, 19 (57,1%) pacientes tinham o tipo generalizado, sendo quatro (14,3%) em localização acrofacial e 12 (42,9%) vulgar. Outros 12 pacientes (42,9%) tinham o tipo localizado, dos quais quatro (14,3%) em padrão focal e oito (28,6%) segmentar (tabela 1).
Para melhor análise estatística e avaliação mais precisa da correlação entre as variáveis, classificamos as áreas envolvidas e tratadas em tronco, face e área cervical e extremidades superiores e inferiores. O resultado da repigmentação também foi classificado em ruim a moderado e bom a excelente. As frequências dos locais afetados e tratados são mostradas na tabela 1.
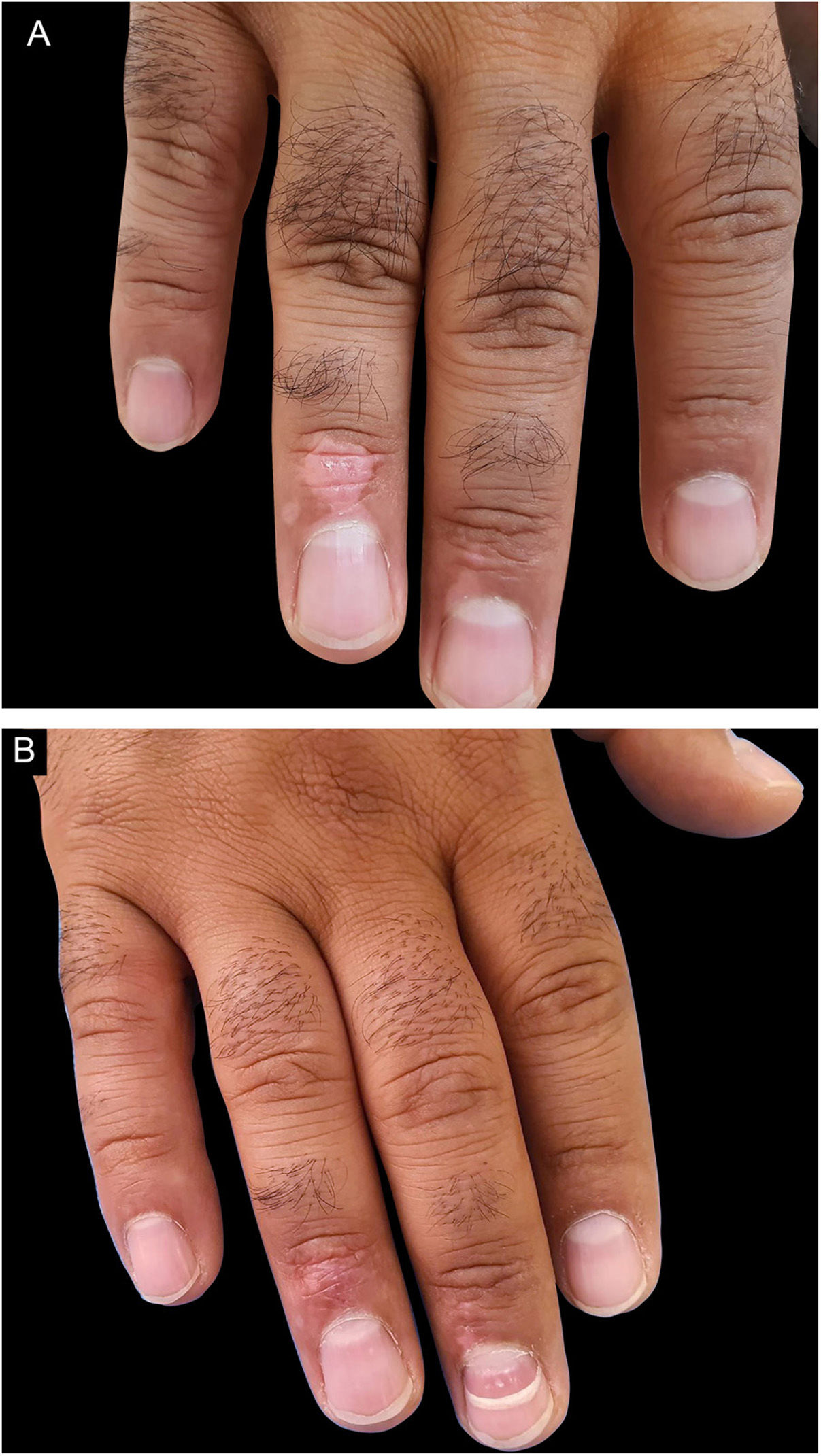
As frequências dos locais tratados com mais detalhes incluíram os dedos das mãos, 15 (13,9%), tórax, 12 (11,1%), área genital, 11 (10,2%) e região bucinadora, nove (8,3%). As outras áreas tratadas estão listadas na tabela 2.
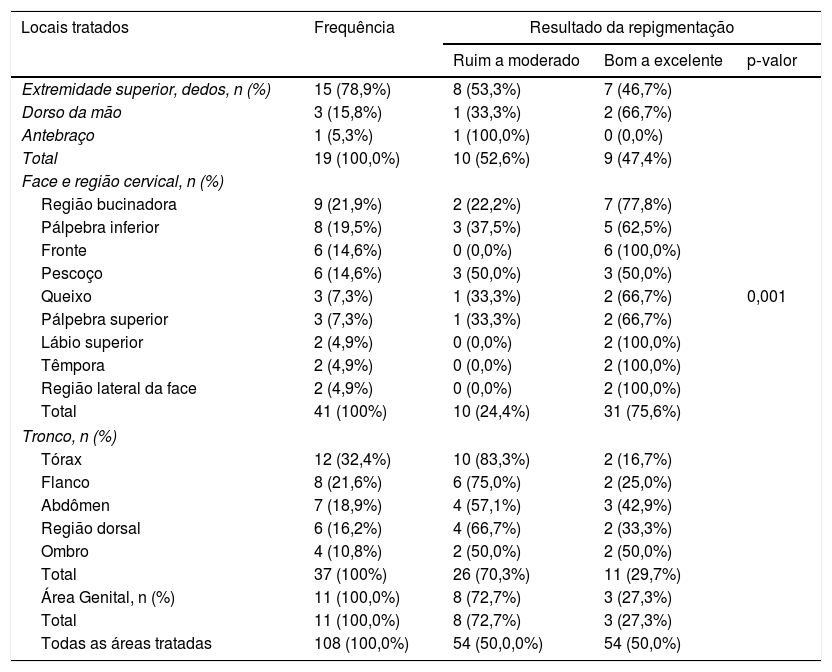
Locais tratados e resultados de repigmentação nos pacientes do presente estudo
| Locais tratados | Frequência | Resultado da repigmentação | ||
|---|---|---|---|---|
| Ruim a moderado | Bom a excelente | p‐valor | ||
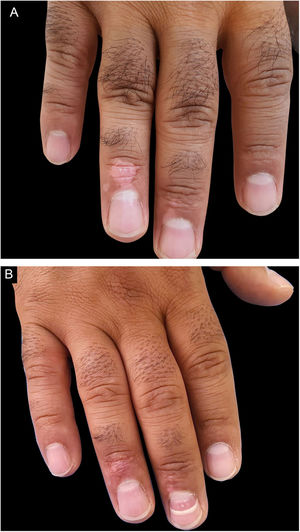
| Extremidade superior, dedos, n (%) | 15 (78,9%) | 8 (53,3%) | 7 (46,7%) | |
| Dorso da mão | 3 (15,8%) | 1 (33,3%) | 2 (66,7%) | |
| Antebraço | 1 (5,3%) | 1 (100,0%) | 0 (0,0%) | |
| Total | 19 (100,0%) | 10 (52,6%) | 9 (47,4%) | |
| Face e região cervical, n (%) | ||||
| Região bucinadora | 9 (21,9%) | 2 (22,2%) | 7 (77,8%) | |
| Pálpebra inferior | 8 (19,5%) | 3 (37,5%) | 5 (62,5%) | |
| Fronte | 6 (14,6%) | 0 (0,0%) | 6 (100,0%) | |
| Pescoço | 6 (14,6%) | 3 (50,0%) | 3 (50,0%) | |
| Queixo | 3 (7,3%) | 1 (33,3%) | 2 (66,7%) | 0,001 |
| Pálpebra superior | 3 (7,3%) | 1 (33,3%) | 2 (66,7%) | |
| Lábio superior | 2 (4,9%) | 0 (0,0%) | 2 (100,0%) | |
| Têmpora | 2 (4,9%) | 0 (0,0%) | 2 (100,0%) | |
| Região lateral da face | 2 (4,9%) | 0 (0,0%) | 2 (100,0%) | |
| Total | 41 (100%) | 10 (24,4%) | 31 (75,6%) | |
| Tronco, n (%) | ||||
| Tórax | 12 (32,4%) | 10 (83,3%) | 2 (16,7%) | |
| Flanco | 8 (21,6%) | 6 (75,0%) | 2 (25,0%) | |
| Abdômen | 7 (18,9%) | 4 (57,1%) | 3 (42,9%) | |
| Região dorsal | 6 (16,2%) | 4 (66,7%) | 2 (33,3%) | |
| Ombro | 4 (10,8%) | 2 (50,0%) | 2 (50,0%) | |
| Total | 37 (100%) | 26 (70,3%) | 11 (29,7%) | |
| Área Genital, n (%) | 11 (100,0%) | 8 (72,7%) | 3 (27,3%) | |
| Total | 11 (100,0%) | 8 (72,7%) | 3 (27,3%) | |
| Todas as áreas tratadas | 108 (100,0%) | 54 (50,0,0%) | 54 (50,0%) | |
O resultado da repigmentação da pele foi bom a excelente em 54 (50,0%) e ruim a moderado em 54 (50,0%) manchas tratadas, respectivamente (tabela 2).
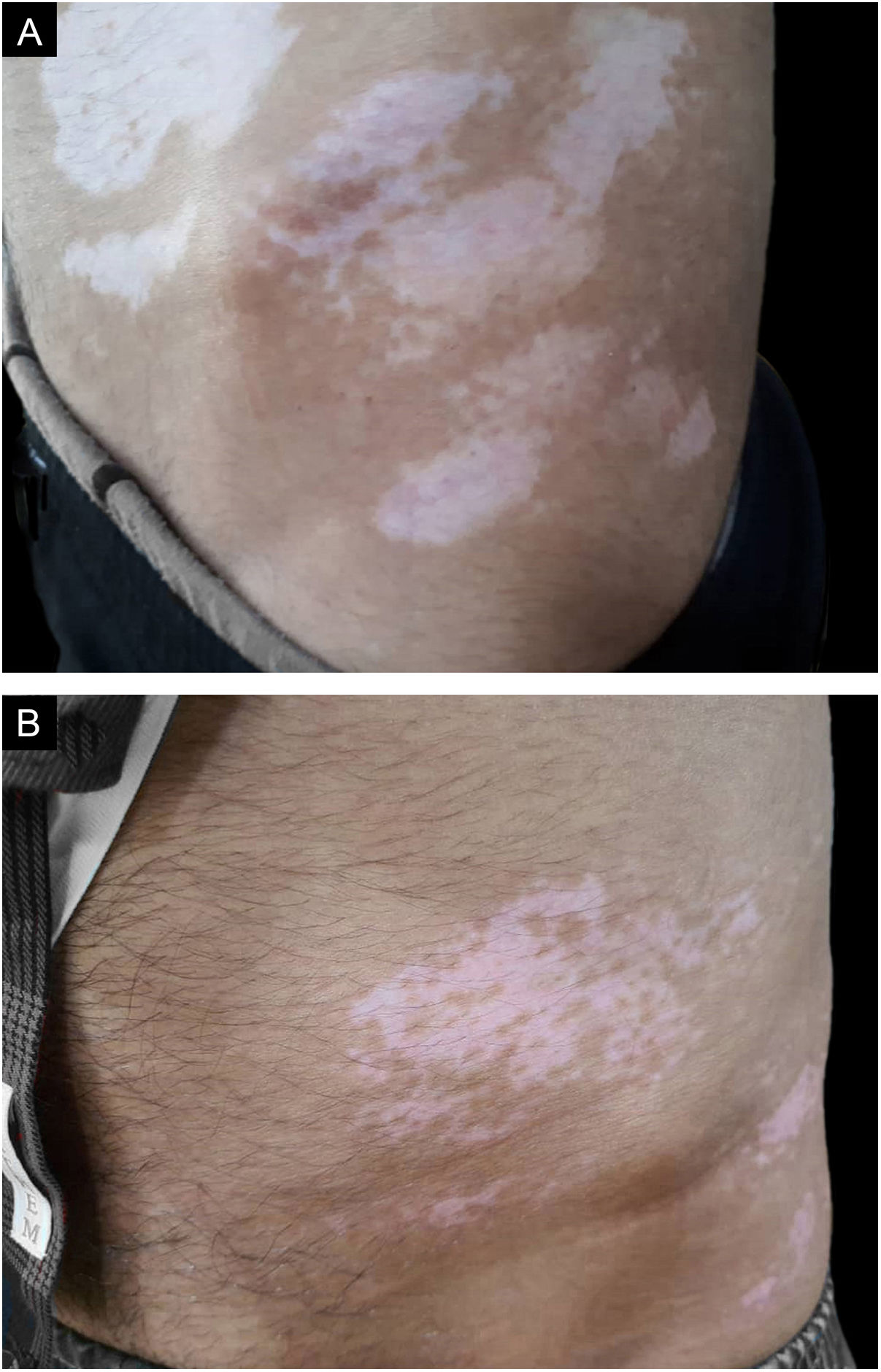
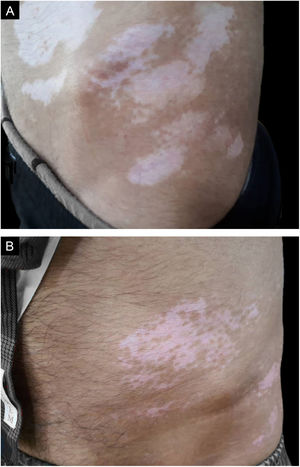
Boa a excelente repigmentação de manchas de vitiligo na face e área cervical, tronco, extremidade superior e área genital foi observada em 31 (57,4%), 11 (20,4%), nove (16,7%) e três (5,5%) pacientes, respectivamente (tabela 2).
Repigmentação ruim a moderada de manchas de vitiligo na face e área cervical, tronco, extremidade superior e área genital foi observada em dez (18,5%), 26 (48,1%), dez (18,5%) e oito (14,8%) pacientes, respectivamente (tabela 2).
Houve relação significativa entre o resultado da repigmentação e o local tratado (p > 0,05). Face e área cervical apresentaram repigmentação significativamente melhor que as outras áreas (p < 0,05; tabela 2).
Prurido, queimação, eritema, hiperpigmentação pós‐inflamatória e vesículas como complicações do presente estudo foram observadas em 24 (22,2%), 21 (19,4%), 14 (13,0%), dez (9,2%) e quatro (3,7%) locais tratados, respectivamente. Todas essas complicações foram transitórias e melhoraram após dois meses.
Fenômeno de Koebner, discromia e cicatrizes inestéticas não foram encontrados em nenhum local, receptor ou doador.
DiscussãoOs achados do presente estudo revelaram que a ANTMG é um procedimento eficaz, simples e seguro para o tratamento do vitiligo, especialmente a forma recalcitrante. A ANTMG também demostrou um resultado de tratamento significativamente melhor na face e área cervical.
A maioria de nossos pacientes, com média de idade de 25,93 ± 7,11 anos, era do sexo feminino (71,4%), tinha vitiligo do tipo generalizado (57,1%) e foi submetida a ANTMG comumente na face e área cervical (38%).
O presente estudo, consistente com a maioria dos estudos,12,17–21 não mostrou diferença significativa entre o resultado do tratamento de manchas de vitiligo através de ANTMG e idade, duração da doença e sexo.
Embora o tipo limitado de vitiligo tenha mostrado uma resposta significativamente melhor em relação ao tipo generalizado no tratamento com ANTMG em estudos anteriores,6,10,18 nos pacientes do presente estudo, ambos os tipos clínicos de vitiligo não tiveram diferença importante no resultado do tratamento. Considera‐se muito importante selecionar os pacientes com vitiligo adequadamente e realizar o procedimento com precisão para obter resultados de tratamento aceitáveis em qualquer tipo clínico de vitiligo.
Estudos relataram resultados variáveis para ANTMG no tratamento do vitiligo, variando de resultados ruins a excelentes.5–18 A competência na realização no procedimento ANTGM é um fator importante para alcançar um resultado satisfatório no tratamento. Nesse procedimento, o uso de instrumentos médicos especiais, o método de coleta de materiais nos sítios doadores, a preparação do local receptor e as terapias adjuvantes após a cirurgia podem afetar o resultado do tratamento.6,7,13,14,18
O local das manchas de vitiligo, o tipo de vitiligo e a estabilidade e recalcitrância da doença são outros fatores importantes envolvidos na obtenção de um resultado aceitável.5,6,9,10,12,14,18
Nossos achados revelaram que 50% dos locais com vitiligo tratados apresentaram resultado bom a excelente, um resultado de tratamento aceitável. As vantagens do presente estudo foram que todos os pacientes apresentavam uma forma resistente da doença e a maioria dos pacientes apresentava a forma generalizada de vitiligo e áreas de difícil tratamento, como área acral e genital, o que poderia ter afetado negativamente os resultados do tratamento.
Consistente com a maioria dos estudos, 6,10,13,18 nossos pacientes apresentaram algumas queixas como prurido e hiperpigmentação pós‐inflamatória (HPI) no sítio receptor após o procedimento, mas todas foram transitórias e melhoraram após várias semanas.
Uma das principais preocupações era a possível ocorrência de despigmentação, isto é, o fenômeno de Koebner na área doadora, o que foi observado em alguns estudos, mas não no nosso, indicando a seleção adequada de pacientes e a estabilidade do vitiligo nesses pacientes.
ConclusãoCom a seleção adequada de pacientes com vitiligo, a ANTMG é um procedimento seguro e de baixo custo com resultado satisfatório no vitiligo recalcitrante. O treinamento adequado dos médicos e a experiência dos especialistas no emprego do método podem ser determinantes para aumentar a taxa de sucesso. Sugere‐se a realização de estudos futuros em vários centros com mais casos e mais variáveis.
Suporte financeiroNenhum.
Contribuição dos autoresIraj Ghorbani: Concepção e planejamento do estudo; revisão crítica da literatura.
Mozafar Khazaei: Participação intelectual em conduta propedêutica e/ou terapêutica de casos estudados; revisão crítica do manuscrito.
Hossein Kavoussi: Aprovação da versão final do manuscrito; participação efetiva na orientação da pesquisa; participação intelectual em conduta propedêutica e/ou terapêutica de casos estudados; concepção e planejamento do estudo.
Ali Ebrahimi: Participação intelectual em conduta propedêutica e/ou terapêutica de casos estudados; elaboração e redação do manuscrito.
Mansour Rezaei: Obtenção, análise e interpretação dos dados; análise estatística.
Reza Kavoussi: Elaboração e redação do manuscrito; obtenção de dados.
Kamran Mansouri: Revisão crítica da literatura.
Conflito de interessesNenhum.
AgradecimentosOs autores gostariam de agradecer ao Student Research Committee e a todos os funcionários do Deputy of Research and Technology da Kermanshah University of Medical Sciences, Kermanshah, Irã.
Este artigo é o resultado da tese de um aluno.
Como citar este artigo: Ghorbani I, Khazaei M, Kavoussi H, Ebrahimi A, Rezaei M, Kavoussi R, et al. Treatment of recalcitrant vitiligo by autologous non‐cultured and trypsinized melanocyte grafting in the west of Iran. An Bras Dermatol. 2022;97:315–20.
Trabalho realizado na Kermanshah University of Medical Sciences, Kermanshah, Irã.